第82回 ハダカデバネズミと老化研究
1.はじめに
ハダカデバネズミは、普通のネズミ(マウス、ラット、ハムスター等)と比べ極めて長寿であることが知られているが、最近、中国の研究者らにより、長寿の手掛かりとなるcGASという遺伝子とその変異について画期的な研究成果が報告された。
今回はそれを巡る経緯や意義、課題等について分析・考察を行うこととする。
2.ハダカデバネズミと老化
(1)ハダカデバネズミとは
ハダカデバネズミ(Heterocephalus glaber)は、アフリカのエチオピア、ケニア、ジブチ、ソマリア等に生息するげっ歯類である。
頭部が大きく、飛び出た歯を持ち、全身がピンク色でしわしわで、体の表面には細かい体毛しか生えておらずつるつるである。属名のHeterocephlus(変わった頭部)、種小名のglaber(無毛の)、また日本語名「ハダカデバネズミ」は、そうした特徴に由来している。
ハダカデバネズミは、他のげっ歯類とは違い、アリやハチのような集団生活を営む。地中にモグラのようにトンネルを掘り、その奥で、繁殖を行う女王を中心にコロニーを形成して生活している。地中で一生を過ごすため視力はほとんどなく、また、哺乳類であるにもかかわらず体温を調節できないという特徴を持つ。
しかし、ハダカデバネズミが注目されているのは、何といっても、他のげっ歯類に比べ、寿命が際立って長いことだろう。マウスやラットの寿命が2~3年であるのに対し、ハダカデバネズミの寿命はなんと30年近い。10倍以上にもなるのである。そして、彼らは多くの老化関連の疾患に対し、驚くほどの耐性を持っている。特に、これまでがんが見つかったことは一度もないのである。

(2)ハダカデバネズミに関するこれまでの研究経緯
ハダカデバネズミは上記のような特徴のため注目を集め、世界中の多くの研究者らが、その長寿や疾患抵抗性のメカニズムを解明するため研究を行ってきている。
ハダカデバネズミの長寿の原因については、いろいろ議論がなされている。当初から指摘されたのが、彼らは厳しい環境にさらされた場合には、自らの代謝を低下させて生き延びるという特性を持ち、それが代謝での酸化による自身のDNAの損傷を防いでいるというものだ。
また、通常、老化細胞内には神経伝達物質セロトニンが蓄積しており、それから生じる過酸化水素(H2O2)が細胞へのダメージを引き起こすが、ハダカデバネズミの細胞にはそのような蓄積は見られず、セロトニンが蓄積されないメカニズムを備えていることが推測される。
さらに、がんの抵抗性の理由についても議論がある。ハダカデバネズミはがん抑制遺伝子の産物であるp53タンパク質の濃度がマウスに比べて50倍も高く、それががん細胞の分裂速度を遅くしたり、接触抑制すなわち他の細胞と接触すると分裂を停止する働きを強めることに関わっていると推測される。
ハダカデバネズミの細胞から分泌される大量のヒアルロン酸が、がん細胞の周囲を取り囲むことで、がんの増殖を防いでいるという指摘もある。
このように、ハダカデバネズミの長寿等の原因としていろいろな説があるが、その遺伝子構造はネズミよりもむしろヒトに近いこともあり、ハダカデバネズミのゲノム解読・解析にも努力が払われてきた。老化に関連するさまざまな遺伝子やその産物であるタンパク質を、他のネズミやヒトの配列と比較し、その違いが寿命とどう関係するのか調べようという試みである。今回の研究もその一環である。
3.今回の研究について
今回、研究成果を報告したのは中国上海市にある同済大学(中国の科学技術のHPにある同済大学の記事を参照されたい)の研究者らである。本年10月のサイエンス誌に発表された。
彼らは、cGAS(Cyclic GMP-AMP synthetase(環状グアノシン1リン酸ーアデノシン1リン酸合成酵素))という生体物質が、ハダカデバネズミにおいて、ヒトやマウスとは異なる独自の進化を遂げているのではないかという仮説を立てた。
ヒトを含む多くの哺乳動物において、cGASは二つの働きを持つことが知られている。
一つは細胞内に異常なDNAがあると活性化し、免疫反応を誘導することによって、異常DNAを排除して細胞を防御する働きである。それがcGAS本来の機能だとされている。
だがもう一つ、cGASにはDNAの二重らせん構造が誤って切断された際に修復を行うメカニズムである「相同組換え修復」を阻害する働きがある。ただ使い物にならなくなった細胞のDNA修復を阻害し、死滅させるのはいいのだが、中途半端に働くと異常修復、ひいてはがんや細胞老化につながることになる。
つまりcGASは、異常の起きた細胞を守って生きながらえさせる働きと、細胞に細胞死や老化を促すという、正反対の働きを併せ持っているのである。
彼らは、ハダカデバネズミのcGASの遺伝子やタンパク質を詳細に分析した。そうして、ハダカデバネズミのcGASには、ヒトやマウスのcGASとは異なる4つのアミノ酸置換があることを突き止めた。
そして彼らは、ハダカデバネズミのcGASをヒトとマウスの細胞に導入した。すると、これらの細胞ではDNA修復能力が顕著に向上し、細胞の老化を示すマーカーが減少することが分かった。一方、cCASを完全に除去した細胞ではDNA損傷は蓄積した。
このため、彼らはこの4つのアミノ酸の変化がcGASの機能を劇的に変化させていると考えた。ハダカデバネズミのcGASは、他の哺乳動物のcGASとは逆に、DNAの相同組換え修復を促進する働きを持っていると推測した。そして、ハダカデバネズミのcGASが、この4つのアミノ酸置換によって、DNA修復時に分解されにくくなっていることがその要因であると考えたのである。
彼らにより提唱されたメカニズムとして、下図のうち右上の2つの枠を見てもらいたい。
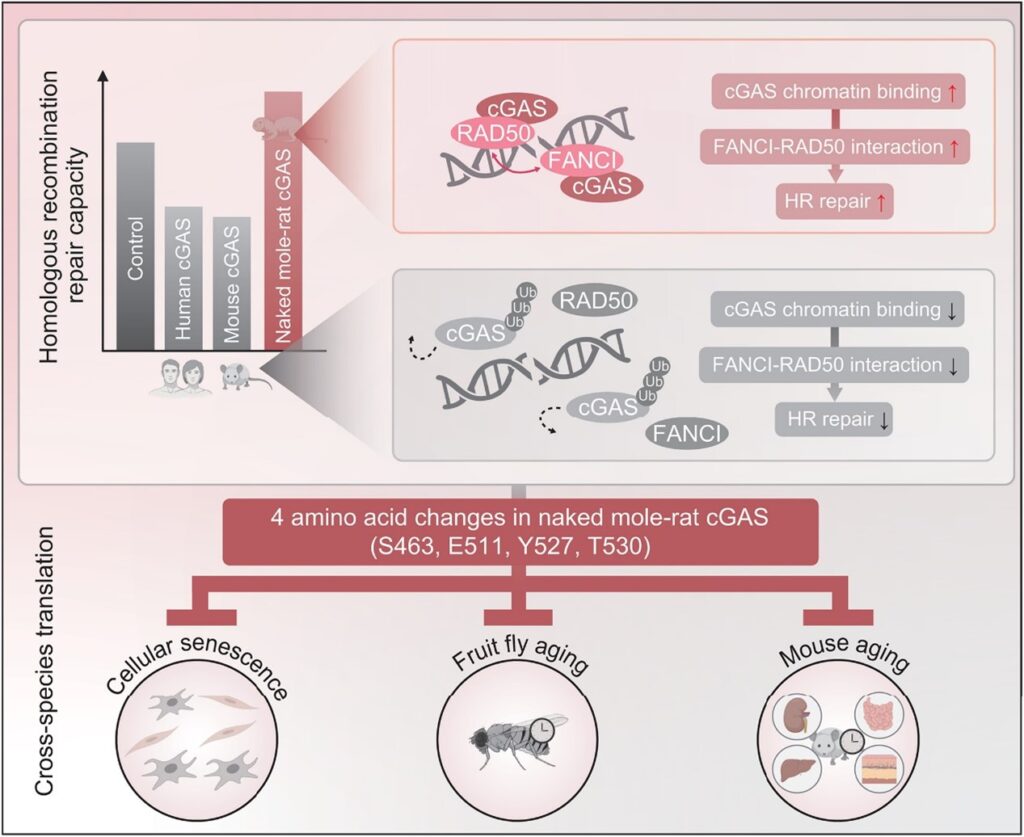
本来、DNAの相同組換え修復時には、FANCIやRAD50といった修復因子が働く必要があり、それを損傷部位に持ってきて働かせるためにはcGASがクロマチンに結合している必要がある。ところが、ヒトやマウスのcGASはユビキチンと結びつくことでcGASはクロマチンに結合しにくくなり、その働きが抑制されている。
一方、ハダカデバネズミのcGASは、これら4つのアミノ酸の変化によりユビキチン化されにくくなり、しっかりFANCIやRADが働けるよう、クロマチンに長時間結合できるようになっていたのである。
彼らは実験動物も用いてその検証を進めた。
まず、ハダカデバネズミに特異的な4つの変異を含むcGASを発現するように改変されたショウジョウバエが、ヒト版cGASを発現するショウジョウバエよりも長生きすることを示した。
さらに、遺伝子導入技術を用いて、ハダカデバネズミのcGASを高齢のマウスで発現させた。すると、マウスの活動が活発になり、様々な臓器の老化細胞の数が減少した。これは、ハダカデバネズミのcGASが、個体レベルでの老化の進行を遅らせ、健康寿命を延ばした可能性を示唆している。
4.本研究の意義と課題
今回の研究では、ハダカデバネズミの長寿の原因について、cGASのアミノ酸配列が他の動物と異なっていることが有力であることが、培養細胞やいくつかの実験動物モデルによって検証された。これに倣い、ヒトについても、cGASのアミノ酸を改変することで、DNA修復能力を高め、老化を遅らせることができる可能性がある。
だが、今回の発見がヒトの老化治療に実際に応用されるのは、技術的にも、倫理的にもまだまだ先のことになるだろう。
今回、研究チームは、細胞やショウジョウバエを用いた機能実験において、外来侵入者や細胞ストレスによって活性化される自然免疫反応を抑制するcCASのヒト変異体を用いた。
先述のように、cGASは本来、DNAを感知して免疫反応を引き起こす重要なセンサーでもあるが、今回の実験ではそれを考慮せず、DNAの修復のみに焦点を当てている。このため、cGASの機能を改変することによって、異常細胞の生存を助け、感染症への抵抗力や、がんに対する免疫が損なわれたりする可能性も否定できない。
一連のメカニズムについて、系統的・網羅的に研究を進めることにより、より効率的で安全な遺伝子改変による寿命の伸長を目指す必要がある。
さらに、実際に遺伝子改変による延命が実用化されるに際して、倫理的問題として、はたして極端な長寿が許されるか、また許されるとしても、それがヒトにとって幸せなのかという問題が出てくるだろう。
単純にハダカデバネズミと一般のネズミの寿命の比較がヒトに適用された場合、800歳や1,000歳という寿命のヒトが出現することを意味する。少々SF的である。
これは疾患の治療のような正当性があるかどうか分からない。むしろ、知能とか身体能力の高度化という、現在の法令では制限されている改変の類になるだろう。
そして個人間の差別の問題、生活スタイルの問題、社会経済的な問題等、検討しなければならないことが山ほど生じてくるに違いない。
5.おわりに
不老不死は人類の永遠の夢である。
著者は学生時代、卒業研究の担当教官に「先生、どこかで不老不死の研究を行っている研究室はありますか?」という質問をしたことがある。するとその教官は、「私はそんな研究を行っている研究室は知らない。しかし、生命科学の全ての研究はそれを目指していると言える。基礎研究も、がんなどの病気を治す研究もそうだ。そうした研究が最終的に積み重なって、最終的に不老不死が実現されていくと思う。生命科学の全ての道は不老不死に通じる。」そう答えられた。
その後40年以上経ったが、今更ながら、その言葉はけだし名言だと感じざるを得ない。
ゲノム全解読等による老化関連遺伝子の探索、iPS細胞等を用いた再生医療、人工知能(AI)の利用等、さまざまな生命科学の知見を用いることで老化の本体解明や寿命の大幅な延長につながることが期待され、さらに、実際の適用に当たっては生命倫理の発達なくして難しい。そうした、生命科学全体の発達がなされた先に、不老不死の世界が見えてくることを期待する。
ただし、その時には先述のように大きな社会的議論が巻き起こるとは思うが。
参考文献
・Y. Chen et. al. (2025) “A cGAS-mediated mechanism in naked mole-rats potentiates DNA repair and delays aging”, Science; Vol.390,
・M. Basu, “Naked mole rats live for decades — genetic tweaks reveal insights into ageing”, (2025/10/9) Nature HP
(https://www.nature.com/articles/d41586-025-03279-y)
・山形方人「【新研究】不老不死を分子で読む-ハダカデバネズミの4つのアミノ酸の秘密」(2025/10/13)NEWS picks HP
(https://newspicks.com/news/15261969/body/)
・「ハダカデバネズミ」ウイキペディア
(https://ja.wikipedia.org/wiki/%E3%83%8F%E3%83%80%E3%82%AB%E3%83%87%E3%83%90%E3%83%8D%E3%82%BA%E3%83%9F)
ライフサイエンス振興財団理事兼嘱託研究員 佐藤真輔

