第92回 仮想細胞による細胞分裂のシミュレーションモデルの作製
1.はじめに
米国イリノイ大学の研究者らからなるチームは、細菌をシミュレーションしたバーチャル(仮想)細胞モデルにより、細胞分裂の過程を近似することに成功し、今年3月、セル誌に発表した。今回はこのことについて、背景、経緯、意義等を含め、分析・考察する。
2.今回の研究を巡る背景
バーチャル細胞によるシミュレーションの試みについては、以前ニューズレターでも紹介したが(第74回 将来の実験はバーチャル細胞で)、以下、簡単にレビューする。
バーチャル細胞とは、現実の細胞を模してコンピュータ上に作られた仮の細胞のことである。
バーチャル細胞に関するこれまでの主な取組としては、日本では1996年に慶応大学で行われた「電子化細胞(E-cell)プロジェクト」がある。同プロジェクトではマイコプラズマをモデル生物として、その維持に必要な127個の遺伝子を選んでコンピュータ上でモデル化した。するとバーチャル細胞はブドウ糖を取り込み、タンパク質を合成して自己を維持した。これは細胞の一部の過程をシミュレーションした原始的なものだったが、当時としては画期的なものだった。
また海外では、2012年、米国スタンフォード大学の研究者らにより、525個の遺伝子を持つマイコプラズマ・ジェニタリウムの内部構造を踏まえた計算モデルが作製された。これにより、先のE-Cellプロジェクトにより構築されたものよりいっそう複雑な内容をシミュレーションすることができた。
これらの試みは、各生体物質すなわち遺伝子、RNA、タンパク質の機能をそれぞれ仮想細胞の中で再現させることにより、細胞のメカニズムを模したモデルを構築しようとするものだった。
ただしそのためには各生体物質の機能を解明するとともに、それぞれの相互作用も把握しておかねばならず、前提となる膨大な知識が必要だった。また、こうしたモデルでは細胞内部を単純で均一な化学反応器として扱うことが多かったが、実際の細胞は高密度で混沌とした環境にあり、分子は細胞内に局在しつつ移動する中で衝突して化学反応を起こすという、複雑なメカニズムである。
このため、これまでは、最も遺伝子数の少ないマイコプラズマでも、バーチャル細胞として一定の機能を維持させていくのが精いっぱいだった。しかしそれでも細胞の成長、分裂や増殖の過程のシミュレーションは難しく、ましてや構成要素が格段に増える真核細胞や多細胞でのシミュレーションは極めて困難とされてきた。
なお、このようなメカニズム重視のバーチャル細胞のモデルとは別に、AIを用いたバーチャル細胞作りも行われはじめた。すなわち、ゲノム、RNA、タンパク質等、時間系列で調べた細胞内の生体物質の全データを取り込むことで、個々の生体物質間の正確な関係やメカニズムが分かっていなくても、それをうまく成り立たせるようなモデルを構築するのである。こちらはまだまだ研究途上であるが、研究者らはその構築を支援するための、シングルセル(単一細胞)でのデータセットを大量に作製、公開して相互に利用するようになってきている。
3.今回の研究について
(1)本研究の手法
今回、米国イリノイ大学の研究者らからなるチームが目指したのは、上記の2つのタイプのバーチャル細胞のうち、メカニズム重視型のものである。彼らはそのような細胞を構築することで、従来のものよりさらに進め、細胞分裂の過程までも再現させることを目指した。
対象とする細胞として、マイコプラズマのうち、マイコプラズマ・ミコイディスが選ばれた。そして、そのバーチャル細胞については、細胞の成長と分裂をプログラムし、調整するために、必要な最小限の遺伝子を持つように設計することとした。つまり、サイズを小さくすることで、シミュレーションの複雑さを軽減しようとしたのである。
同細菌のゲノムには本来900個ほどの遺伝子が存在するが、バーチャル細胞のゲノム作製に当たっては、必要性が高い493個の遺伝子に絞り、それ以外の400個以上の遺伝子は除外した。そのような遺伝子の選定や、そのRNAやタンパク質等の機能の付与や位置づけに際しては、これまで培ってきた膨大な知見や実験データが利用された。同研究チームは既にマイコバクテリアについて、20分間の成長のみをモデル化したシミュレーションを発表していたが、その成果も利用された。そうして作製されたバーチャル細胞はJCVI-syn3Aと名付けられた。
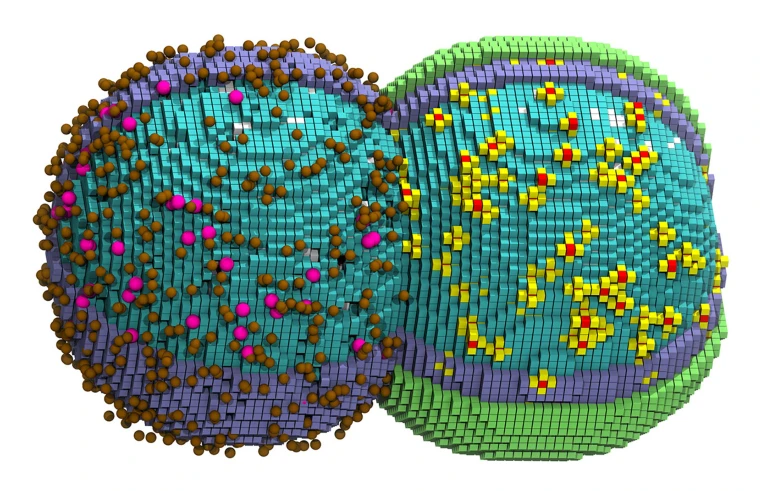
そして同研究チームは、JCVI-syn3A中でDNA、タンパク質、リボソーム、その他の分子が時間とともに変化する様子を模倣する3D(時間まで含めると4D)シミュレーションモデルを作製した。
このモデルにおいては、機能がよく解明されている特定の分子、たとえばDNA複製酵素等については、実際の活動の測定に基づき、規則に従うように設計された。そして、相互作用可能な分子どうしが物理的に接近すると、反応が起こるようにした。
一方、細胞の生存に必要な遺伝子のうち、数十個の遺伝子の機能はまだ正確に解明されていなかったが、それらは不活性な球体としてモデル中に組み込んだ。また、実際の細胞では、複数のリボソームが同じmRNAの転写産物に結合して同時にタンパク質を合成していくが、複雑であるため、本モデルではmRNA分子1つにつきリボソーム1つが対応して結合するような仕組みにした。
そして、細胞分裂を模倣できるようにするため、研究者らは3つのフェーズを1つに統合した。
1つ目はDNAの分裂のフェーズ。これはDNAを単なる情報列としてではなく、形状と動きをもつ実態として扱った。バーチャル細胞内で、複製が進むにつれて染色体が変化し、徐々に分離していく様子を模倣させた。
2つ目は化学反応のフェーズ。微小な空間の中で飛び回る分子を再現させ、衝突により分子反応を起こす過程を模倣させた。
3つ目は細胞の経済状態のフェーズ。分子が動き回り、DNAが分裂していく間、細胞の栄養とエネルギー状態が監視できるようにした。
こうして、3つのフェーズをうまく連動して働かせることにより、成長するバーチャル細胞が分裂の準備が整うまで生き延びるのに十分な栄養とエネルギーが確保できるようにしようとしたのである。
(2)本研究の経緯と結果
上述のように、研究者らの目標は、JCVI-syn3Aが自己複製して2つに分裂する過程、つまり細胞周期と細胞分裂をシミュレーションすることだった。だが、初期の試みは、DNA分子が生成されるよりも速く分解したり、細胞膜から噴出したりしたため、失敗に終わった。
そこで彼らは、そうした問題に対処するため、上述の3つのフェーズの統合・連動を含め、各種微調整を行った。すると、仮想モデルは、細胞が分裂する際に、膨脹したり伸長したりする様子等、実際の生命活動の多くの詳細を再現できるようになり、ついには細胞分裂の様子を見事に模倣したのである。
バーチャル細胞が分裂するのに要した時間は105分で、それは実際の細胞が分裂するのに要する時間と極めて近かった。また、細胞中でDNAの複製だけでも51分かかることが推定された。
ただし、この105分間のシミュレーションにはスーパーコンピュータで6日間を要し、このような細胞モデルの実行がいかに計算負荷の高い活動であるかを浮き彫りにした。
なお、このシミュレーションでは、生きた細胞を忠実に再現し、その隠されたつながりで明らかになったところも多かった。たとえば、細胞が利用できるエネルギーが遺伝子の読み取りを直接制御する仕組みをこのモデルは正確に示した。また、新たなDNAを複製するにはそのためのDNAの構成要素が必要で、それが不足すると遺伝情報の読み取りプロセス自体が滞り、速度が低下した。
4.本研究の意義・今後の展望
(1)本研究の意義
このシミュレーションは、従来のバーチャル細胞ではできなかったような、細胞分裂等の細胞活動を実に広範な範囲で正確にとらえている。前述の成長のみのシミュレーションモデルに比べても、大きな進歩を示している。シミュレーションの時間枠を細胞周期全体にまで延長することで、細胞プロセスをより詳細に観察することが可能になった。
そうなると、直接的な実験では不可能な仮説を検証することもできるようになりそうだ。たとえば成長条件を変えたり、抗生物質や細胞分裂を阻害する他の薬剤で処理したりする等、変化する条件下での細胞の挙動を研究する道が広がる。
また、こうした細胞シミュレーションは、あらゆるレベルの学生に細胞内の生物学的複雑性を説明するのに役立つ優れた教育ツールにもなる。
ただ、現段階ではJCVI-syn3Aはまだ研究開発段階である。今後、細胞周期を通してこれらのプロセス全てを整合的に動作させることは大きな課題である。
(2)メカニズム重視型とAI利用型の今後の展望
2で述べたように、今回のように、生化学の詳細な規則をモデルに組み込んでいくメカニズム重視型のバーチャル細胞を作製する取組みとは別に、AIを用いてバーチャル細胞を作製する取組みがある。
AIによって生成されるバーチャル細胞の目標は、大量の細胞生物学的データについて、個々の分子の機能は分かっていないという前提の下、一からAIに学習させることで、生命の内部構造を近似することである。しかし、そのために要するデータ量は、時間変化も考慮するとなると、極めて膨大になる。AIが生成するバーチャル細胞が実現するには10年かかるという意見もある。
その点、このようなメカニズム重視型のバーチャル細胞の場合、既に解明されている分子の機能はそのまま活用するため、はるかに効率がよい。JCVI-syn3Aシミュレーションや、スタンフォード大学が大腸菌向けに開発している同様のモデルは、AIモデルほど多くのデータを必要とせず、容易に検証可能な生化学的メカニズムに基づいて作製されている。
ただ、今後のAIやスパコンの進展により、どうなるかは分からない。また、AI利用型とメカニズム重視型を併用していくという選択肢もあると考えられる。
5.おわりに
もうずいぶん前の話になるが、かつて著者が参加した一般向けの講演会のことである。
同講演会では、当時最速を誇った日本のスパコン「京」による、さまざまなシミュレーションについてプレゼンがなされていた。講演者は、京がいかに優れているか、これまでできなかったどんなことができるようになるかを、具体例をもとに聴衆に話し、質問にもよどみなく答えていた。
そこで著者は、「これにより細胞そのもののシミュレーションは可能になりますか。」と質問した。
すると講演者は途端に顔をしかめ、しばらく沈黙した後、次のように答えた。
「いやあ、生物のメカニズムは実に複雑なので、京でシミュレーションできるのはごく一部の化学的・物理的な反応だけです。もし細胞全体をシミュレーションするなら、ペタ(10の15乗)では全然無理で(ちなみに「京」は10ペタ)、エイコサ(10の18乗)でも難しいかもしれませんね。」
当時の知見としてはこの回答は妥当であり、また、講演者は正直だったと思う。それほど細胞のシミュレーションは難しいものだった。しかし、今回のように、分子レベルで機能等が十分明確化されているものについては、そのデータを組み込んでいくことにより、また、AIもあわせて活用すれば、案外、より高度・複雑な細胞でもシミュレーションが可能になるのではないか。そう期待しつつ今後もフォローを続けていきたい。
参考文献
・Z. R. Thornburg et. al. (2026) “Bringing the genetically minimal cell to life on a computer in 4D”, Cell; Vol.189, 1-16
・E. Callaway (2026) “‘Virtual cell’ captures the most-basic process of life: bacterial division” Nature; Vol.651
・T. Tarita “Scientists Simulated an Entire Living Cell in 4D and Watched It Divide” (2026/3/19), ZME Science HP
https://www.zmescience.com/science/virtual-cell-life-cycle-simulated
・“From 1 cell to 2, researchers have simulated the entire cell division process” (2026/3/19), NSF HP
https://www.nsf.gov/bio/updates/1-cell-2-researchers-have-simulated-entire-cell-division
ライフサイエンス振興財団理事兼嘱託研究員 佐藤真輔

