第4回 ゲノム編集~ノーベル賞と特許を巡る争い・その1
ゲノム編集技術は生命科学やその応用分野に大きな進展をもたらす革命的技術だが、その特許を巡っては長年紛争が続いている。本年2月、米国特許庁(USPTO)が、ゲノム編集技術CRISPR/Cas9に関する2回目の特許紛争の判決を出したというニュースがあった。これに関し、これまでの経緯や周辺状況を含め2回に分けて解説したい。
ゲノム編集とは遺伝子の特定部分をピンポイントで改変する技術である。遺伝子の人為的な改変としては、古くは1950年代に、DNAに放射線を当てて品種改良をする方法が用いられるようになり、また1960年代になると、制限酵素すなわちもともと生体内にあるDNAを特定の塩基配列部位で切断するタンパク質が次々と発見され、1970年代になると、それを用いて人為的に遺伝子改変した生物が作られるようになった。
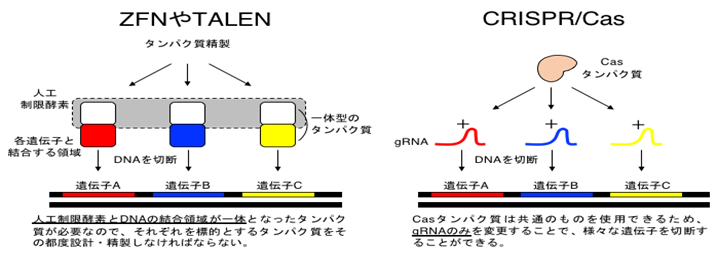
しかし1990年代になって、さらにピンポイントで遺伝子を改変する技術が生まれた。それがゲノム編集技術で、1996年にZFN、2010年にはTALENという方法が開発された。ただ、それらは特定の塩基配列を標的とすることを目的として、人工の制限酵素とDNAの結合領域が一体となったタンパク質が必要で、その設計と精製は標的配列毎に行わねばならず、時間と経費がかかり、しかも遺伝子編集に成功する確率も低いという問題があった。
その後もよりよいゲノム編集方法を目指した研究が進んだ結果、2012年にCRISPR/Cas9が発表された。これは各遺伝子に結びつくRNAと切断を行うCasタンパク質を組み合わせたもので、もともと自然界にあった「細菌の獲得免疫機構」を利用したものだった。RNAの合成は比較的簡単で、かつCasタンパク質は共通のものを使うため、製造までの期間や費用が大幅に節約され、しかも精度が高くなった。ちなみに自然界では、標的DNAに結びつくcrRNAと、Cas9との相互作用に関わるtracrRNAという2つのRNAが必要で、これを合わせてガイドRNA(gRNA)と呼ぶが、ゲノム編集技術として開発されたものは一般にこの2つのRNAを一体化した「一分子型ガイドRNA(sgRNA)」が用いられる。
この研究に大きく貢献したのが、米国カリフォルニア大学バークレー校(UCB)のジェニファー・ダウドナ博士のチームと、ブロード研究所(ハーバード大学とMITが共同で設立した研究所)のフェン・チャン(Feng Zhang、張鋒)博士のチームであった。2つのチームは重要な国際賞を幾つか獲得し、ノーベル賞を激しく争った。例えば、ダウドナ博士とその共同研究者のシャルパンティエ博士は2017年に日本国際賞を、一方のチャン博士は2018年に慶應医学賞をそれぞれ受賞している。また3名とも、ノーベル賞の前哨戦とも言われるガードナー国際賞を2016年に同時受賞している。
両チームは、最初のCRISPR/Cas9に関する論文をいずれもScience誌に投稿しており、これらが掲載された時期がダウドナ博士らのUCBチームが2012年6月、チャン博士らのブロード研のチームが2013年1月であったことから、最終的には2020年にダウドナ博士とシャルパンティエ博士がノーベル化学賞を受賞した。
ノーベル賞受賞では決着がついたものの、ゲノム編集技術の特許については複雑な状況が続いている。論文投稿と並行して、米国特許庁(USPTO)に対し、UCBチームとブロード研はそれぞれCRISPR/Cas9のゲノム編集技術の出願を行った。論文と同様、本出願日もUCBチームが2013年3月15日、ブロード研が同年10月15日と、UCBが先行した。ところが、ブロード研がUSPTOに「迅速承認」を要請した結果、2014年4月、同研究所に先にいくつかの特許が与えられた。
このような結果となった背景には、米国の特許制度の運用変更が大きく影響したと言われている。同国ではかつて、先発明主義つまり同技術を早く発明した者に対し、特許を与えていた。だがそれではいつ発明したかについての証拠の検証が困難で、曖昧さが残る。このため同国では2013年3月から、欧州等と同様、先願主義すなわち先にUSPTOに出願した者に優先して特許を与えることとしたのである。
今回のCRISPR/Cas9のゲノム編集技術に関する特許は、まさに同制度の切り替え時期に行われたものであった。ブロード研側は、特許の内容をうまく絞り込み、それをUSPTOに仮申請などで持ち込んだ。UCB側は、より広範な内容を盛り込んで特許を取得しようとしたこともあって、迅速承認システムを利用しなかったことにより、結果としてブロード研側に先に特許が認められたのである。
ただ、USPTOの判断根拠は不明である。USTPOが両者の特許申請が重複していない、つまりブロード研は真核細胞に対するCRISPR/Cas9を目的とした申請であり、UCB側は特に生物を限らずsgRNAを用いるCRISPR/Cas9を目的とした申請と判断した可能性もあるが、ブロード研側が研究者の実験ノートを提出し、UCB側より早く同技術を発明(先発明主義)していた根拠を示したともされており、このあたりの曖昧さが両者の対立に拍車をかけることになった。
それから約3年後となる2016年2月、UCB側が「真核細胞におけるCRISPR/Cas9を利用する発明は私たちの方が早い」というインターフェアレンス(特許抵触審査)を宣言した。インターフェアレンスとは、一番先に発明した人を認定するために司法判断を仰ぐシステムである。
そもそも、アカデミックの研究機関どうしがここまで対立して特許紛争を起こすのは前例のないことだった。アカデミックどうしであれば、本来なら特許抵触での訴訟沙汰になる前に、互いに合意に達するのが普通だと考えられる。だが、CRISPR/Cas9特許のもつ市場価値は大きく(数億ドル~数十億ドルとされる)、そしてすでに両研究機関ともに、同技術を用いたスピンオフ企業を設立し、それに自身が保有する又はすることになる特許についての専用実施権を与え、関連する特許業務を行わせていた。このような事情で両者とも引くに引けなくなってしまったのである。
USPTOは2017年2月に判決を下し、すでにブロード研に与えた特許の判断を支持し、UCB側から提起されたインターフェアランスには当たらないとした。ブロード研のCRISPR/Cas9システムの発明は真核生物に限定されるのに対し、UCB側の発明はsgRNAだが真核生物に限定されない(原核生物やin vitroでの環境も対象としたもの)として、両者の発明は異なるものであるとしたのである。つまり同判決はブロード研の特許を認めつつ、UCB側の特許申請も認められる可能性に言及したのである。
UCBはそれを不服として米連邦巡回区控訴裁判所に異議申し立てしたが、同裁判所は2018年9月にそれを却下する判定を下した。しかし、両者の特許争いはこれで終わらなかった。続きは、次回の記事で述べたい。
(参考文献)
・(九州大学附属図書館)2020年ノーベル化学賞!! 最新のゲノム編集技術「CRISPR/Cas」について: ゲノム編集の歴史とCRISPR/Cas9
(https://guides.lib.kyushu-u.ac.jp/CRISPR/Cas9/introduction)
・知財コラム「ゲノム編集 特許紛争~ノーベル化学賞の裏で~」
(https://pasona-kp.co.jp/column/detail/9)
2022年8月10日
ライフサイエンス振興財団嘱託研究員 佐藤真輔

