第34回 ヒトES細胞からのヒト胚モデルの作製
イスラエルの研究者らは本年9月、ヒトES細胞(胚性幹細胞)からヒト胚によく似た構造体を作製するのに成功したと、Nature誌に発表した。この研究は、イスラエルのワイツマン研究所のグループが行った研究である。今回はこの研究の内容とその背景や問題点等について説明する。
実験ではナイーブ型ヒトES細胞が使われた。
ES細胞は、胚の発生の途中段階である胚盤胞の中に塊として存在する細胞を取り出したもので、基本的にエピブラストという細胞を経て胎児のあらゆる組織に分化する性質を持つが、胎児を包み込む胎盤等には分化できない。このようなES細胞をプライム型ES細胞と呼ぶ。
しかし、このプライム型ES細胞の培養条件を工夫することにより、胎盤等を含む全組織への分化が可能となり、これをナイーブ型ES細胞と呼ぶ。
イスラエルのチームは、このナイーブ型ES細胞を用い、それに化学物質を働かせることにより、ヒト胚の初期段階で見られる4種類の細胞、すなわち
①エピブラスト細胞(胚・胎児そのものになる)
②原始内胚葉細胞(卵黄嚢になる)
③胚外中胚葉細胞(栄養膜の内側を覆う)
④栄養膜細胞(胎盤になる)をそれぞれ誘導した。
そうしてできた細胞を、合計120個になるよう、一定の比率で混合し、培養した。
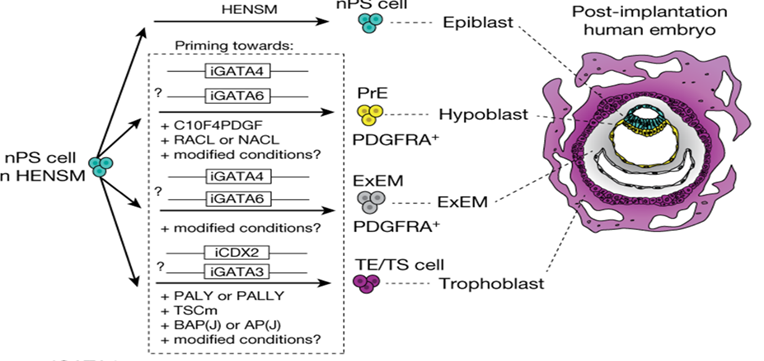
すると、そうして試みたうちの約1%は、ヒト胚に似た集合体を形成したのである。この集合体は、胎盤や卵黄嚢といった構造物が、適正な形や大きさで、正しい位置に形成され、培養後8日目には、受精後14日目のヒト胚に極めて似た構造になった。
胎盤になる栄養膜が胚を包んでいるのが観察され、また、胎児に栄養を送る際に母親の血液で満たされる、ラクナと呼ばれる空洞も観察された。さらに、妊娠検査薬で陽性反応を示すシグナルを出していることも確認された。
こうした、いわゆるヒト胚のモデル作りに関しては、最近、次々に研究成果が発表されている。Nature誌には、イスラエルのチーム以外にも、英米の2チームが、それぞれナイーブES細胞を用いてヒト胚モデルを作出したとする論文が掲載された。
このうち英国ケンブリッジ大学のチームは、ES細胞を特殊な条件で培養し、胚モデルを作ることに成功した。培養開始から4日ほどで、受精から9日ほど経った本物のヒト胚と同じような構造になった。その後、羊膜など、着床後に作られる組織や細胞と同じような特徴の細胞も確認できたとしている。
また、米国エール大学のチームも同様に受精後9~14日目ごろに似たヒト胚モデルを作成したと発表した。
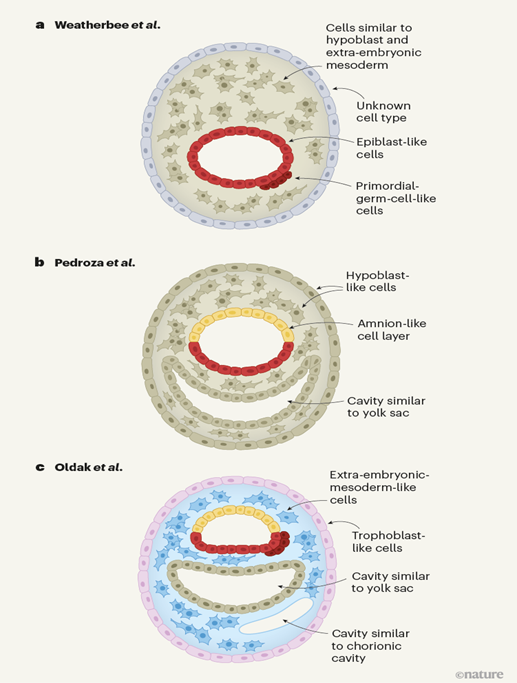
上から順に、英国ケンブリッジ大学、米国エール大学、イスラエルのチーム(Nature誌より)
これらを含め、この1~2年で少なくとも6件の胚モデルの研究が発表されており、非常にホットな研究領域になっている。ただ、今回のイスラエルのグループの研究成果は、対応するヒト胚の時期やその構造から、よりヒト胚の実態に迫ったモデルであると言える。
なお、以前のニュースレター「第22回 ES細胞から作出したサルの胚を子宮に移植」でも紹介したが、ヒトではないものの、中国の研究チームはサルのES細胞を18日目まで培養し、胚盤胞様の構造の作出に成功しており、さらに、それをサルの子宮に移植して妊娠反応を起こさせている。
こうしたヒト胚モデルの研究の意義は何か。一言でいえば、初期の発生過程の解明である。
受精卵は、受精後最初の数週間に劇的に変化するため、その詳細はまだ謎の部分も多い。このため体外で段階的に観察・分析を行うことが効果的だが、それを支持する胎盤等の環境がないと、ある時期以上の発生は技術的に難しい。
ヒト胚を胎盤まで疑似したモデルを用いることにより体外で安定的に培養・観察・分析することができれば、それを通じて得ることのできる科学的・医学的知見は計り知れない。
そうした解明を通じ、流産の防止につながる。受精卵は、受精後母親の子宮に着床し、胎児に育つ。しかしその過程は失敗が多く、胚の半数強は着床前後の段階でうまく育たなくなり、流産になるとされている。ヒト胚モデルを通して何が流産の原因になるかを知ることは大いに意義がある。
ただし、先述のようにヒト胚モデルの作成の成功率は低く(1.09-1.64%)、現段階で流産防止云々を論ずるのは時期尚早である。また、このモデルでは、胚の子宮内膜への着床は含まれておらず、受精から発生までの全過程を再現することはできていない。
また関連するが、新生児の先天異常の原因の究明を行うことも期待される。医薬品の臨床試験では妊婦は通常除外され、医薬品の胎児への影響は、一般的に薬の作用機序から判断される。ヒト胚モデルを使用することにより、直接的にヒト胚に対する薬物の副作用、特に催奇形性等を評価できるようになるかもしれない。
さて、こうした技術的論点のほか、ヒト胚について欠かせないのは倫理的論点である。
これまでヒト胚に関しては、臓器などの形成が本格化する受精後14日を超えてヒト胚を研究室で培養してはならないという、いわゆる「14日ルール」があった。
しかし2021年5月、国際幹細胞学会(ISSCR)がガイドラインを改定し、条件付きで14日を超える培養を認めた。正確には、各国・地域で社会的支持が得られ、政策や規制で容認されれば、体外での14日を超えての生育の必要性・正当性についての検討が可能とされた。
同ガイドラインは、ヒト幹細胞の研究、臨床応用、および関連する研究活動について規定しているが、同改定時には、ヒト胚モデルに対しても、一般の胚と同等か、それに倣った倫理的配慮をするべき旨の方針が示された。
これに関し、各国政府は検討を始めているが、その方向性は様々である。
オーストラリアではヒト胚モデルを一般のヒト胚と同じやり方で研究規制すると決定しているのに対して、日本、英国、米国は少なくとも現時点で両者を同等とはみなしていないようである。
まだ機能的に同等であることが科学的に立証されていないため別扱いとしてよいという立場と、将来的には機能的に同等になる可能性があるなら両者を同じ扱いにすべきだという立場の対立がある。
日本では、広島大学、京都大学、東京大学の研究者が2022年9月、「ヒトブラストイド(ヒト胚モデル)の研究規制のあり方」についての論文をEMBO report誌に発表した。同論文では、ヒト胚モデルが一般的なヒト胚と同等の発生能力を持つか否かという論点に加え、ES細胞とiPS細胞のどちらの細胞から胚モデルを作るか等も研究規制に影響を与えうることを指摘し、規制をめぐる倫理的立場とその限界について論じている。
日本政府は、こうした国内外の動きも踏まえ、ヒト胚モデルを使う研究をどう規制するべきか議論を始めている。専門家による作業部会を設けてヒト胚モデルの定義や、本物のヒト胚との共通点や違いを整理した上で、ヒト胚モデルを作製・利用する上でのルールについても検討していくことになると思われる。
このように、ヒト胚モデルに関しては、内外における研究面、規制面ともにかなり動きがあり、着実なフォローアップが必要であると思われる。
(参考文献)
・J. Rossant & J. Fu “Why models with caution”, Nature; Vol.622, 454-456
・N. Moris “Stem cell model a two-week- old human embryo”, Nature; Vol.622, 469-470
・木村正人「ヒトの受精卵そっくりの「合成胚」の研究はどこまで許されるか?」(2023/9/20)(https://surfvote.com/issues/iwkmzknrzf0s)
・ジェイムズ・ギャラガー「精子と卵子使わずヒト胚に近い「胚モデル」を作製 イスラエルの研究チーム」BBC NEWS JAPAN(https://www.bbc.com/japanese/66728134)
・茜灯里「卵子も精子も使わずに「発生後2週間のヒト胚モデル」作成、構成要素も完全再現・・・倫理問題クリアで不妊治療に貢献か」ニューズウィーク日本版(2023/9/15)(https://www.newsweekjapan.jp/akane/2023/09/2-1.php)
ライフサイエンス振興財団嘱託研究員 佐藤真輔

