第73回 プライム編集による初の臨床試験が行われる
1.はじめに
本年5月、米国プライム・メディシン社は、慢性肉芽腫症(CGD)という希少疾患に対し、ゲノム編集技術の一つであるプライム編集による初の臨床試験を行ったことを発表した。
今回はその内容や背景、意義等について分析・考察する。
2.プライム編集とは
(1)従来のゲノム編集
プライム編集を含むゲノム編集技術については、本ニューズレターでも何度か紹介してきたが、簡単におさらいする。
CRISPR/Cas9をはじめとするゲノム編集技術は、当初、目的とする原因遺伝子のところでDNA二本鎖を両方とも切断し、遺伝子の機能を喪失させる方法として開発されてきた。だがこの方法だと二本鎖切断に伴う修復時の誤りが起きたり、遺伝子の本来の働きまで喪失してしまったりする懸念があった。
それを改善したのが塩基編集(CRISPR2.0)である。これは遺伝子の1文字(塩基)を置換して修復する方法であり、二本鎖を完全に切断するのではなく、片側の鎖だけを切断して一塩基の置換ができるようになった。
しかし、この方法でも、一塩基の置換だけにとどまり、複数の塩基置換を行ったり、さらに、ある程度の大きさのDNA断片を導入したりすることはできなかった。
そうなると疾病の治療等に適用できる範囲は限定されてしまい、これまでCRISPR/Cas9技術が実際に市場化されているのは、鎌状赤血球貧血病とβサラセミアという2つの血液疾患に対する治療法にとどまっている。たとえばテイ・・サックス病という遺伝性疾患は、典型的な原因としてHEXAという遺伝子に4文字のDNAが挿入されて生じる。そのような疾病には従来のゲノム編集技術は無力だった。
(2)プライム編集
これに対し、プライム編集は、ある程度の大きさを持つDNA配列を正確に導入する手法として、塩基編集を開発したハーバード大学の同じ研究室で、2019年に開発された。
プライム編集は、DNA二本鎖を切らないタイプの変異Cas9に、RNAからDNAを転写する逆転写酵素をつなげた融合Cas9タンパク質と、通常のgRNA配列に逆転写酵素の鋳型となるRNA配列を付加した長めのgRNAであるprime editing gRNA (pegRNA)を組み合わせたものを用いる。このpegRNAの配列のうち、標的DNAに相補的な配列の部分と、 DNA合成用の足場となる配列と、編集したい配列の鋳型となる部分を、目的に応じて自分で設計して使用することになる。
実際の編集過程では、細胞の中でプライム編集ツールが発現すると、まず変異Cas9とpegRNAが複合体を形成する。pegRNAは標的DNA配列のところまで変異Cas9を運んでいき、DNAの片方の鎖だけ切断する。
すると、切断されたDNA領域の配列と、それと相補的な配列を持つpegRNAのプライマー結合配列の部分とが結合し、逆転写酵素がpegRNAの鋳型となる部分の配列を基にして一本鎖DNAを合成する。
この新たに合成された一本鎖DNAが、標的DNAの切れ込み部分に挿入され、最終的にDNA配列の書き換えが完了する。
このように、プライム編集の作用機序は少し複雑かもしれないが、DNA二本鎖切断が伴わないため、望まれない変異の導入を避けて新たな配列の挿入や欠損を導入できる画期的な方法だといえる。
なお挿入できる大きさは40塩基程度までとなっていたが、最近の報告によると、プライム編集ツールを活用し2種類のペアとなるpegRNAを用いることで、DNAドナー配列を供給することなく最大1kbもの配列の挿入をすることも可能になってきている。
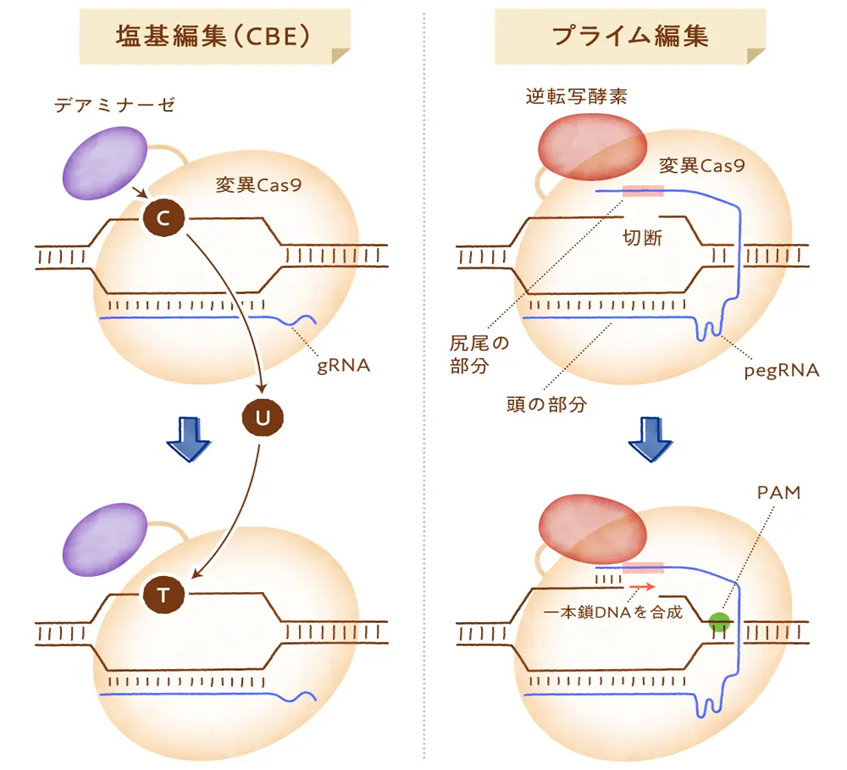
(日本医学会連合ゲノム編集解説ウエブサイトより)
3.今回の臨床試験について
(1)本臨床研究の位置づけ
プライム・メディシン社は、米国マサチューセッツ州に拠点を置くバイオテクノロジー企業である。同社はプライム編集技術を用いた治験薬PM359を、慢性肉芽腫症(CGD)の成人及び小児患者に適用した。
2024年5月に、PM359は米国食品医薬品局(FDA)からオーファンドラッグ、すなわち希少医薬品として優先的に承認審査される旨の指定を受け、臨床試験に入った。現在第Ⅰ/Ⅱフェーズ多国籍臨床試験として、安全性、生物学的活性、及び予備的な有効性の評価を目的として行われている。
(2)慢性肉芽腫(CGD)について
CGDは、免疫系のうちの顆粒球、特に病原体を直接貪食する好中球の酵素遺伝子の変異によって発症する疾患である。変異が起こるのは、NADPH酸化酵素複合体のサブユニットをコードする各種遺伝子である。典型的な変異はCYBA、CYBB、NCF1、NCF2、CYBC1又はNCF4遺伝子に発生し、遺伝子変異の種類により5つのタイプ(変異型)に分類される。
CDGが発症すると、免疫系が弱まり、生命を脅かす可能性のある細菌感染症や真菌感染症、そして治療困難な炎症性疾患に罹患しやすくなる。
治療法としては現在のところ骨髄移植しかないのだが、患者は移植片対宿主病(GVHD)すなわち移植されたドナーの臓器が免疫反応により患者の臓器を攻撃したり、移植不全が起きたりするリスクがあり、それを防止するため、免疫型が高度に一致したドナーを確保することが大きな課題となっている。
(3)臨床試験の方法
今回の臨床試験は、NCF1遺伝子のdelGT変異、つまりGとTの二塩基が欠失することにより生じるCGDを治療するために行われた。この変異はCGDのp47phox変異型で最も多くみられる疾患原因変異であり、CGD症例全体の約25%に関与しているという推測がある。
治療方法は、患者自身の血液細胞を取り出してプライム編集を行い、それを患者に戻す、いわゆる自家体外造血幹細胞療法である。患者は編集されてできたPM359を静脈内に投与され、投与前、投与後15日目、及び投与後30日目にNADPH酸化酵素の活性を測定された。
(4)臨床試験の結果
その結果、第一例となった10代の少年について投与後1か月経過した時点での発表となったが、PM359投与により、15日目までに好中球の58%、30日目までに好中球の66%でNADPHオキシダーゼ活性が完全に回復したことが明らかになった。これは、臨床的に効果があるとみなされる20%を大幅に上回るものだった。
そして、患者に戻された造血幹細胞は急速に生着し、14日目に好中球、19日目に血小板の生着が確認された。他の承認済みの遺伝子編集技術では、同じ測定基準で生着はそれぞれ27日目と35日目であることから、その約2倍の速さで生着したことになる。
さらに安全面ではこれまで深刻な副作用等は見られていない。
(5)今後の予定
今回の発表はあくまで中間段階でのものである。治験が成功したかどうかを判定するためには、改変した幹細胞自体が真に増殖しているかを6か月から1年かけて確認していく必要がある。
なお、プライム・メディシン社は、PM359の臨床データを発表すると同時に、今後、CGDについては独自の取組みを進める予定はないことも明らかにした。同社はPM359の臨床開発を社外で継続する選択肢を検討しているとのこと。
4.おわりに~今後のゲノム編集
ゲノム編集技術はゲノム上の目的の位置で正確かつ安全に編集を行えるということで当初から注目され、着実にその守備範囲を広げてきている。特に今回、わずか2塩基の置換・挿入とはいえ、プライム編集技術をはじめてヒトに適用したことの意義は大きい。
ただし、先述のように、現在のプライム編集で編集・挿入可能な塩基数はせいぜい40個くらいまでであり、遺伝子や遺伝子群を導入し、各種疾病を根本から治療するのはまだまだである。
今後、複数のプライム編集の要素を組み合わせた方法、また、ニューズレターでも紹介した、動く遺伝子を用いる方法(第35回 ゲノム編集を用いた遺伝子治療が進展)、藻類由来のプロテアーゼを用いる方法(第63回 新たなゲノム編集技術により重い代謝疾患の乳児が治癒か)等を含め、いっそうの技術開発に期待したい。
一方、ゲノム編集による治療、特に今回のような自家移植は個別化医療として、多額の費用がかかる。実際に市場化されているものでも1回の治療で約200万ドルかかるとされる。このため特に希少疾患ではせっかく開発してもなかなか患者に用いられない可能性があり、開発のモチベーションがあがらない。上記、プライム・メディシン社の自社のみでの試験継続断念もそれが一因かもしれない。
今後、iPS細胞にもならい、細胞バンクの整備や、拒絶反応が起こらないよう操作された細胞の利用等により、コスト低減化に取り組んでいくことも必要と思われる。
参考文献
・“News Release Details”, (2025/5/19), Prime Medicine HP
(https://investors.primemedicine.com/news-releases/news-release-details/prime-medicine-announces-breakthrough-clinical-data-showing)
・“Ultra-powerful CRISPR treatment trialled in a person for first time”, Nature; Vol.641, 1083
・K. O’Hanlon Cohrt“First-Ever Prime-Editing Therapy Shows Safety and Efficacy in Patient With Chronic Granulomatous Disease”(2025/5/21), CRISPR Medicine News(https://crisprmedicinenews.com/news/first-ever-prime-editing-therapy-shows-safety-and-efficacy-in-patient-with-chronic-granulomatous-dis/)
・ジャンルカリッチョ「遺伝学、プライム編集で人を治癒:世界初」FUTURO PROSSIMO HP
(https://ja.futuroprossimo.it/2025/05/genetica-prime-editing-cura-una-persona-prima-volta-al-mondo/)
・「5.2新たなゲノム編集技術開発の現状」日本医学会連合ゲノム編集解説ウエブサイト
(https://www.jmsf.or.jp/genome/5-2.php)
ライフサイエンス振興財団嘱託研究員 佐藤真輔

