第14回 米国でアルツハイマー病治療薬が承認
日米の企業が共同開発をしているアルツハイマー病の治療薬「レカネマブ」が、同疾患の進行を遅らせる効果があるとして、米国において承認された。これにより日本での同薬の承認にも弾みがつきそうである。今回はこれについて解説する。
厚生労働省の統計によると、80代では3人に1人、90代では2人に1人が認知症を発症している。このうち最も多いのがアルツハイマー型の認知症(アルツハイマー病)であり、認知症患者全体の3分の2を占めている。このため同疾患に対する治療薬の開発が希求されてきたが、これまでなかなか効果的なものはなかった。
アルツハイマー病では、脳の神経細胞が壊れ、脳に萎縮が起こることにより認知機能の低下が起こる。そのメカニズムとして、「アミロイドβ」という異常なタンパク質が脳内に蓄積することが原因の一つと考えられてきた。
日本のエーザイ株式会社と米国のバイオジェン社は、このメカニズムに対して直接働きかける薬の開発を目指した。そうして開発されたのが「レカネマブ」である。このレカネマブは、アミロイドβに対する抗体でできている。投与されると脳内でアミロイドβと結びついてそれを取り除く働きがある。これによりアルツハイマー病の進行を抑え、症状の悪化を防ごうというのである。
レカネマブは昨年7月、米国の食品医薬品局(FDA)に迅速承認制度(ファーストトラック)、すなわち緊急性を要するとして通常より審査手続きを簡素化する制度に基づく申請がなされて受理され、審査されていた。
昨年11月30日、サンフランシスコで開催された第15回アルツハイマー病臨床試験会議で、エーザイ社はレカネマブの臨床試験結果を報告した。これは第Ⅲ相ランダム化比較試験というものだった。
同報告によると、臨床試験には日本を含むアジア、北アフリカ、ヨーロッパの計235施設が参加した。50~90歳の参加者1,795人を、レカネマブを投与するグループ(898人)と、体に害のない生理食塩水(プラセボ)を投与するグループ(897人)の2つに分け、2週ごとに1回、点滴により投与した。そして投与開始から18か月後、画像診断等を使って脳の状態を詳しく調べた。また、記憶や判断力等の認知機能や身体活動など、6つの分野で人の能力を評価する臨床認知機能評価(CDR-SB)という指標で認知機能を評価した。
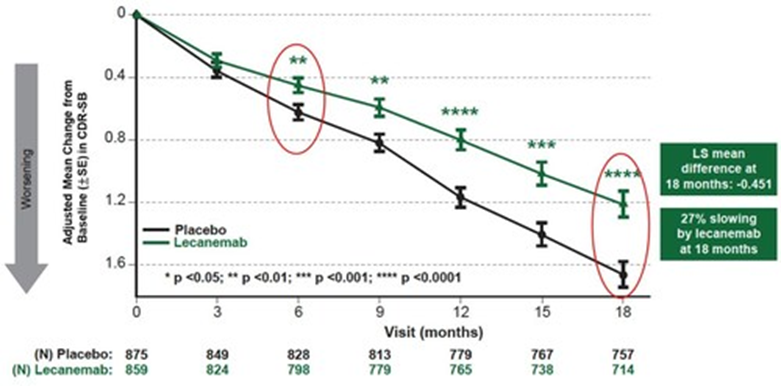
その結果どうなったか。プラセボを投与した患者に比べ、レカネマブ投与した患者はアミロイドβの蓄積量が大きく減った。また、図で見てもらえばわかるが、18か月経った時点でプラセボに比べレカネマブ投与群の認知機能の低下はCDR-SBで平均0.45ポイント良好で、計算すると27%抑えられたことが分かった。プラセボで同様の認知機能の低下を示したのが12か月強の時期であり、それを6か月近く引き伸ばしたことになる。
アルツハイマー病では既にいくつかの薬が普及しているが、それらは病気のメカニズムに直接働きかけるものではなく、大部分は対症療法的なものだった。一時的に症状を緩和させる効果は見られたものの、時間の経過とともに服用前と同様のスピードで認知機能が低下する経過をたどった。
バイオジェン社は少し前、同様にモノクロナル抗体を利用した治療薬として「アデュカヌマブ」を開発した。これもアミロイドβを抗体に結合させて脳から除去するよう設計されていた。同薬についてはFDAで審議され、2021年6月、迅速承認制度で承認されたものの、その後、認知症改善への効果は認められないとの論文が出されたため、販売は進んでいない。また、日本でもアデュカヌマブの承認申請が行われたが、2021年12月に承認が見送られた。
これに対し、レカネマブは同疾患に対し、一定の治療効果を示していると考えられる。ただしFDAは本年1月6日、同薬を承認したのであるが、これは前述の第Ⅲ相試験の結果まで踏まえたものではなく、その前に提出された第Ⅱ相試験データにより判断されたものである。第Ⅱ相試験では、レカネマブが856人の患者の脳のβアミロイドのプラークを減少させることが判明したが、これが患者の認知能力に変化を与えるかどうかは評価されなかった。迅速承認では米国の高齢者向け公的医療保険である「メディケア」の適用制限などから、レカネマブを安価で使用できる患者は限られると考えられる。このため、1月7日、エーザイ社とバイオジェン社は第Ⅲ相試験も踏まえた完全承認を目指し、FDAに申請を行ったと発表した。
日本においても、昨年3月から、医薬品の事前評価相談制度を用いて、臨床試験以外の申請データが医薬品医療機器総合機構(PMDA)に受理されている。米国での承認により、同薬の日本での審査手続きも進むものと考えられ、承認されれば日本初のアルツハイマー治療薬の実用化になる。
なお、承認はされたのであるが、懸念がないわけでもない。昨年11月30日にNature誌に掲載された記事によると、研究者の中にはレカネマブによる治療効果が人の症状に十分顕著な違いをもたらしているかどうか疑問視している者もいる。また、レカネマブで治療された者の約20%は、脳のCTで腫れや出血等の異常を持っていた。さらに、Science誌等では、第Ⅲ相試験で当初プラセボを投与された患者が、その後試験の延長段階でレカネマブの投与を受けたところ3人が死亡した旨報告された。そうであれば、今後本薬が認知機能のそれほど低下していない者に投与される場合、リスクとベネフィットを考慮する必要があるかもしれない。また、レカネマブは米国では1年間で26,500ドルかかるとされており、完全承認されたときには保険適用の範囲をどうするかという課題がある。また、薬をいつまで使うのかということもある。
そのような懸念もあるが、アルツハイマー病をはじめとする認知症の社会的なコストは巨額である。慎重な審査も必要ではあるが、社会全体の利益を考えた場合、アルツハイマー病の画期的な新薬のもたらすメリットは大きいと考えられる。
前回のニュースレターで取り上げたNature誌には、「2023年に注目すべき科学イベント」と題する別の記事があり、以下の9項目を予測している。その1項目にアルツハイマー治療薬が取り上げられている。
・mRNAを利用した各種ワクチン開発
・ジェームズ・ウェッブ宇宙望遠鏡(JWST)に続く望遠鏡開発による高度な天体観測
・WHOによる、将来パンデミックを引き起こす可能性のある病原体監視リストの公開
・各国による月探査ミッション
・βサラセミアや鎌形赤血球症に対するクリスパー療法の進展
・COP27で決まった気候変動基金の詳細の検討
・ミューオン、ニュートリノ等の実験科学の進展
・アルツハイマー治療薬の開発
・フィンランドの使用済み燃料貯蔵施設の稼働
人類にとってもアルツハイマー病の克服は大きな課題である。レカネマブの承認はそのための大きな一歩であることに間違いなく、これを契機とした同疾病の研究の進展を期待をもって見守っていきたい。
(参考文献)
・Eisai presents full results of lecanemab phase 3 confirmatory clarity Ad study for early Alzheimer’s disease at clinical trial on Alzheimer’s disease (Ctad) conference(https://www.prnewswire.com/news-releases/eisai-presents-full-results-of-lecanemab-phase-3-confirmatory-clarity-ad-study-for-early-alzheimers-disease-at-clinical-trials-on-alzheimers-disease-ctad-conference-301689627.html)
・M. Prillaman (2022) “Heralded Alzheimer’s dug works – but safety concerns loom”, Nature; Voi.612, 197-198
・「アルツハイマー病治療薬 レカネマブの効果と副作用は?」(https://www.nhk.or.jp/kaisetsu-blog/700/477773.html)
・“The science events to watch for in 2023” Nature HP
(https://www.nature.com/articles/d41586-022-04444-3
・S. Reardon “FDA approves Alzheimer’s drug lecanemab amid safety concerns”, Nature 07 January 2023
(https://www.nature.com/articles/d41586-023-00030-3)
ライフサイエンス振興財団嘱託研究員 佐藤真輔

